Pada saat ini telah ditemukan lebih dari seratus unsur dan
begitu banyak senyawa kimia yang telah disintesis. Bagaimana agar kita mudah
mempelajari unsur-unsur itu? Para ahli kimia telah mengelompokkan unsur-unsur berdasarkan sifat-sifat
kimia dan fisika yang mirip atau sama.
Untuk mempelajari pengelompokan unsur-unsur berdasarkan
sifatnya dapat digunakan tabel periodik unsur.Tabel periodik unsur berkembang
mulai dari cara pengelompokan yang sederhana sampai yang lengkap.Tabel periodik
yangdigunakan sekarang adalah tabel periodik modern yang disusun berdasarkan kenaikan
nomor atom dan kemiripan sifat unsur. Pada tabel periodik modern, unsur-unsur
dikelompokkan dalam golongan dan periode.
Pada tabel periodik unsur, lambang unsur dilengkapi dengan
nomor atomdan massa atom. Dari data tersebut kita dapat menentukan struktur
atom suatu unsur seperti jumlah proton, neutron, elektron, dan konfigurasi
elektronnya.
Dalam tabel periodik unsur kita dapat mempelajari sifat
unsur seperti logam, metaloid, nonlogam, dan sifat periodik yaitu jari-jari,
energi ionisasi, afinitas elektron, dan keelektronegatifan.
A.Perkembangan Tabel Periodik Unsur
Pengelompokan unsur-unsur dimulai oleh Antoine Lavoisier
yang mengelompokkan unsur menjadi logam dan bukan logam. Selanjutnya pengelompokan
unsur berkembang dalam berbagai bentuk dan dikenal dengan Triade Dobereiner,
Oktaf Newlands, Tabel Periodik Unsur Lothar Meyer dan Mendeleev, serta Tabel
Periodik Unsur Modern.
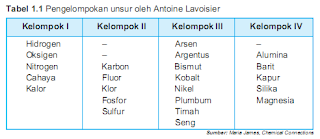
1.Tabel Periodik Unsur Antoine Lavoisier
Antoine Lavoisier
pada tahun 1789, seorang ahli kimia Perancis membagi unsur-unsur menjadi
empat kelompok. Untuk mengenal pengelompokannya, perhatikan Tabel 1.1.
Pada Tabel 1.1 tertera cahaya dan kalor yang bukan unsur.
Pada kelompok IV dimasukkan senyawa yang belum dapat diuraikan menjadi unsur
yang dikenal sekarang.
2.Hukum Triade Dobereiner
J.W. Dobereiner pada tahun 1817 mengelompokkan unsur yang
mempunyai sifat sama, tiap kelompok terdiri dari tiga unsur yang disebut
triade. Untuk mempelajari hukum ini lakukan kegiatan berikut.
Dobereiner mencoba mengelompokkan unsur-unsur yang mempunyai
sifat sama berdasarkan kenaikan massa
atomnya, ternyata didapat keteraturan. Jika tiga unsur diurutkan berdasarkan
kenaikan massa atomnya, maka massa unsur yang kedua sama dengan massa rata-rata
unsur pertama dan ketiga. Pernyataan ini dikenal dengan nama Hukum Triade
Dobereiner.
3.Hukum Oktaf Newlands
Pada tahun 1863, J.W. Newlands mengurutkan unsur berdasarkan
kenaikan massa atomnya. Bagaimana keteraturan yang ditemukannya? Coba
diskusikanpengelompokannya melalui kegiatan berikut!
Dari pengelompokan ini ternyata unsur yang kedelapan
memiliki sifat yang mirip dengan unsur yang pertama, begitu juga unsur yang
kesembilan sifatnya mirip dengan unsur yang kedua, dan seterusnya. Contohnya,
unsur H sifatnyamirip dengan unsur F dan Cl, unsur Li mirip dengan Na dan K,
serta unsur Be mirip dengan Mg.
Pengulangan ini oleh Newlands disebut Hukum Oktaf karena dia membandingkan
pengulangan sifat unsur dengan tangga nada atau oktaf pada lagu. Newlands
memelopori penyusunan unsur-unsur yang sifatnya mirip pada kolom vertikal.
Kelemahan hukum oktaf yaitu pengulangan setiap 8 unsur hanya cocok untuk
unsur-unsur yang massa atomnya kecil. Selain itu masih ada unsur-unsur yang
berimpitan pada urutan yang sama.
4.Tabel Periodik Unsur Lothar Meyer
Pada tahun 1870, Lothar Meyer mencoba membuat daftar
unsur-unsur dengan memperhatikan sifat fisika yaitu volum atom. Dia membuat
grafik volum atom unsur terhadap massa atomnya. Untuk mempelajarinya lakukan
kegiatan berikut.
Pada lengkung Meyer, unsur-unsur Li, Na, K, Rb, dan Cs
menempati kedudukan yang setara, yaitu di puncak. Be, Mg, Ca, Sr, dan Ba berada
di titik kedua dari puncak. Ternyata unsur-unsur yang letaknya setara memiliki
sifat yang mirip
5.Tabel Periodik Unsur Mendeleev
Dimitri Ivanovich Mendeleev pada tahun 1869 di Rusia mengemukakan
hubungan antara massa unsur dengan sifat unsur. Dalam mempelajari keperiodikan
unsur-unsur, Mendeleev selain menggunakan sifat fisika juga menggunakan sifat
kimia.
Pada penelitiannya
seperti New-lands, Mendeleev juga
menyusun unsur menurut kenaikan massa atom relatifnya dan dia menemukan adanya perubahan
sifat secara periodik.
Kelebihan tabel periodik unsur Mendeleev adalah sebagai
berikut.
a.Merupakan sistem periodik pertama yang disusun dalam
bentuk tabel yang terdiri dari delapan lajur vertikal atau golongan dan tujuh
deret horisontal atau periode. Selanjutnya disebut tabel periodik unsur
Mendeleev.
b.Ada tempat yang kosong bagi unsur-unsur yang diramalkan
akan ditemukan dan diberi nama eka boron, eka aluminium, dan eka silikon.
Ramalan tersebut terbukti dengan ditemukannya Scandium (1879), Galium
(1875),dan Germanium (1886). Contoh ramalan Mendeleev untuk Germanium yang
disebut eka silikon tertera pada Tabel 1.2.
Tabel 1.2 Ramalan Mendeleev tentang sifat unsur germanium
c. Dapat menempatkan unsur He, Ne, Ar, Kr, Xe, dan Rn dalam
golongan tersendiri setelah golongan gas mulia ditemukan.
Tabel periodik unsur Mendeleev digambarkan seperti berikut.
Selain keunggulan, tabel periodik unsur Mendeleev mempunyai beberapa kelemahan yaitu sebagai berikut.
a.Ada beberapa urutan unsur yang terbalik jika ditinjau dari
bertambahnya massa atom relatif, misalnya Te (128) ditempatkan sebelum I (127).
b.Triade besi (Fe, Co, Ni), triade platina ringan (Ru, Rh,
Pd), dan triade platina (Os, Ir, Pt) dimasukkan ke dalam golongan VIII. Di
antara unsur-unsur golongan ini hanya Ru dan Os yang mempunyai valensi 8.
6.Tabel Periodik Unsur Modern
Tabel periodik unsur yang digunakan sekarang yaitu Tabel
Periodik Unsur Modern. Setelah tabel periodik unsur Mendeleev, pada tahun 1915
Henry Moseley menemukan nomor atom dan menyusun unsur-unsur dalam tabel
periodik berdasarkan kenaikan nomor atom. Beberapa penelitian menunjukkan
adanya hubungan antara nomor atom dengan sifat-sifat unsur, maka tabel periodik
Mendeleev perlu penyempurnaan. Pada tabel periodik unsur modern unsur disusun dalam
golongan dan periode.
Ada dua sistem yang digunakan pada penomoran golongan yaitu sistem Amerika
dan sistem IUPAC. Sistem Amerika menggunakan angka Romawi I sampai VIII,
masing-masing terdiri dari golongan A dan B. Sistem IUPAC (International Union Pure
and Applied Chemistry) menggunakan angka Arab 1 sampai dengan 18.
Oleh karena sistem penomoran golongan IUPAC belum
memasyarakat dikalangan ahli kimia, maka penggolongan sistem Amerika lebih
banyak digunakan, begitu juga di Indonesia.
Tabel periodik unsur modern digambarkan sebagai berikut.
ARTIKEL TERKAIT:


















kita juga punya nih jurnal mengenai tabel periodik, silahkan dikunjungi dan dibaca , berikut linknya http://repository.gunadarma.ac.id/bitstream/123456789/5424/1/Jurnal.pdf
ReplyDeletesemoga bermanfaat yaa :)